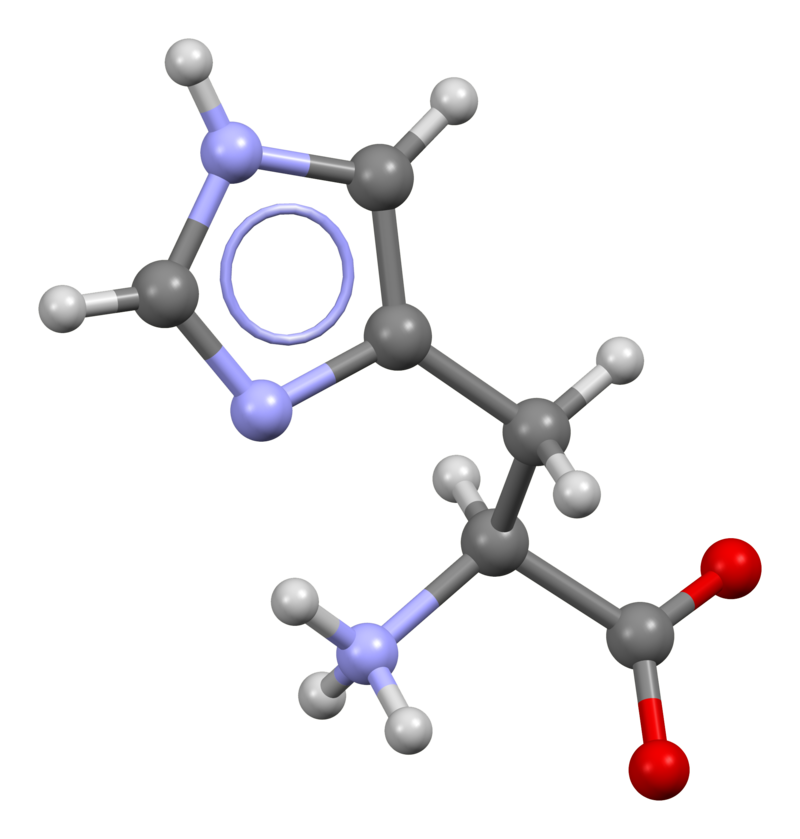
الهيستيدين (His or H) هو حمض أميني ألفا يستخدم في التخليق الحيوي للبروتينات. يحتوي على مجموعة α-amino (الموجودة في شكل –NH3 + البروتوني تحت الظروف البيولوجية) ، ومجموعة حمض الكربوكسيل (الموجودة في شكل –COO− المنسوخ تحت الظروف البيولوجية) ، وسلسلة جانبية إيميدازول (والتي يتم بروتوناتها جزئيًا ) ، وتصنيفه على أنه حمض أميني موجب الشحنة عند درجة الحموضة الفسيولوجية. كان يعتقد في البداية أنه ضروري للرضع فقط ، وقد ظهر الآن في الدراسات طويلة المدى أنه ضروري للبالغين أيضًا.
تم عزل الهيستيدين لأول مرة من قبل الطبيب الألماني ألبريشت كوسيل وسفين جوستاف هيدين في عام 1896. كما أنه مقدمة للهيستامين ، وهو عامل التهابي حيوي في الاستجابات المناعية. جذور الأسيل هي هيستيديل.
الارتباط
يشكل الهيستيدين معقدات تحتوي على العديد من أيونات المعادن. عادةً ما تعمل سلسلة الإيميدازول الجانبية لبقايا الهيستيدين كرابطة في البروتينات المعدنية. أحد الأمثلة على ذلك هو القاعدة المحورية المرتبطة بالحديد في الميوغلوبين والهيموغلوبين. تُستخدم علامات بولي هيستيدين (من ستة أو أكثر من بقايا H متتالية) لتنقية البروتين عن طريق الارتباط بالأعمدة بالنيكل أو الكوبالت ، مع تقارب ميكرو مولار.
ثبت أن ببتيدات بولي هيستيدين الطبيعية الموجودة في سم الأفعى Atheris squamigera تربط الزنك (2+) والنيكل (2+) والنحاس (2+) وتؤثر على وظيفة السموم المعدنية. علاوة على ذلك ، توجد مناطق منخفضة التعقيد غنية بالهيستيدين في بروتينات الربط المعدني وخاصة بروتينات ربط النيكل والكوبالت.
التمثيل الغذائي
التخليق الحيوي
إل-هيستيدين هو حمض أميني أساسي لا يتم تصنيعه في البشر. يجب على البشر والحيوانات الأخرى تناول البروتينات المحتوية على الهيستيدين أو الهيستيدين. تمت دراسة التخليق الحيوي للهستيدين على نطاق واسع في بدائيات النوى مثل الإشريكية القولونية. يتضمن تخليق الهيستيدين في الإشريكية القولونية ثمانية منتجات جينية (His1 و 2 و 3 و 4 و 5 و 6 و 7 و 8) ويحدث في عشر خطوات. هذا ممكن لأن منتج جين واحد لديه القدرة على تحفيز أكثر من تفاعل واحد. على سبيل المثال ، كما هو موضح في المسار ، يحفز His4 4 خطوات مختلفة في المسار.
يتم تصنيع الهيستيدين من فوسفوريبوزيل بيروفوسفات (PRPP) ، وهو مصنوع من ريبوز -5-فوسفات بواسطة ريبوز-فوسفات ثنائي فوسفوكيناز في مسار فوسفات البنتوز. أول تفاعل للتخليق الحيوي للهستيدين هو تكثيف PRPP وثلاثي فوسفات الأدينوزين (ATP) بواسطة إنزيم ATP-phosphoribosyl transferase. يشار إلى ATP-phosphoribosyl transferase بواسطة His1 في الصورة. ثم يحلل منتج الجين الخاص به 4 ناتج التكثيف ، فسفوريبوزيل- ATP ، وينتج الفوسفوريبوزيل- AMP (PRAMP) ، وهي خطوة لا رجوع فيها. يقوم His4 بعد ذلك بتحفيز تكوين phosphoribosylformiminoAICAR-phosphate ، والذي يتم تحويله بعد ذلك إلى phosphoribulosylformimino-AICAR-P بواسطة منتج الجين His6. يقوم His7 بتقسيم فسفوريبولوسيل فورمينو- AICAR-P ليشكل د-إريثرو-إيميدازول-جلسرين-فوسفات. بعد ذلك ، يقوم His3 بتكوين إيميدازول أسيتول-فوسفات يفرز الماء. يقوم His5 بعد ذلك بصنع l-histidinol-phosphate ، والذي يتحلل بعد ذلك بواسطة His2 الذي يصنع الهيستدينول. يحفز His4 أكسدة L- هيستيدينول لتشكيل L- هيستيدينال ، ألدهيد أميني. في الخطوة الأخيرة ، يتم تحويل L- هيستيدينال إلى L- هيستيدين.
تحتاج النباتات ، مثل الحيوانات والكائنات الحية الدقيقة ، إلى الهيستيدين لنموها وتطورها. تتشابه الكائنات الحية الدقيقة والنباتات في قدرتها على تصنيع الهيستيدين. كلاهما يصنع الهيستيدين من بيروفوسفات الفوسفوريبوزيل الوسيط الكيميائي الحيوي. بشكل عام ، يتشابه التخليق الحيوي للحامض الهيستيدين في النباتات والكائنات الحية الدقيقة.
تنظيم التخليق الحيوي
يتطلب هذا المسار طاقة لكي يحدث ، لذلك فإن وجود ATP ينشط الإنزيم الأول للمسار ، ATP-phosphoribosyl transferase (كما هو موضح باسم His1 في الصورة على اليمين). ATP-phosphoribosyl transferase هو المعدل المحدد للإنزيم ، والذي يتم تنظيمه من خلال تثبيط التغذية الراجعة مما يعني أنه يتم تثبيطه في وجود المنتج ، الهيستيدين.
انحلال
الهيستيدين هو أحد الأحماض الأمينية التي يمكن تحويلها إلى مواد وسيطة في دورة حمض الكربوكسيل (TCA) (المعروفة أيضًا بدورة حامض الستريك). يشارك الهيستيدين ، جنبًا إلى جنب مع الأحماض الأمينية الأخرى مثل البرولين والأرجينين ، في نزع الأمين ، وهي عملية يتم فيها إزالة مجموعته الأمينية. في بدائيات النوى ، يتم تحويل الهيستدين أولاً إلى urocanate بواسطة الهيستيداز. بعد ذلك ، يقوم urocanase بتحويل urocanate إلى 4-imidazolone-5-propionate. يحفز Imidazolonepropionase التفاعل لتكوين فورمينوجلوتامات (FIGLU) من 4-imidazolone-5-propionate. يتم نقل مجموعة الفورمينو إلى رباعي هيدروفولات ، وتشكل الكربونات الخمسة المتبقية الغلوتامات. بشكل عام ، تؤدي هذه التفاعلات إلى تكوين الغلوتامات والأمونيا. يمكن بعد ذلك نزع أمين الجلوتامات عن طريق نازعة هيدروجين الغلوتامات أو نقلها لتكوين α-ketoglutarate.
التحويل إلى الأمينات الأخرى النشطة بيولوجيا
حمض الهيستيدين الأميني هو مقدمة للهيستامين ، وهو أمين ينتج في الجسم ضروري للالتهاب.
يحول إنزيم هيستيدين أمونيا-لياز الهيستيدين إلى أمونيا وحمض أوروكانيك. يوجد نقص في هذا الإنزيم في اضطراب التمثيل الغذائي النادر لهستيد الدم ، مما ينتج عنه حمض اليوروكانيك باعتباره نتيجة تشخيصية رئيسية.
يمكن تحويل الهيستيدين إلى 3-ميثيل هيستيدين ، والذي يعمل كمؤشر حيوي لتلف العضلات الهيكلية ، بواسطة إنزيمات ميثيل ترانسفيراز معينة.
الهيستيدين هو أيضًا مقدمة للتخليق الحيوي للكارنوزين ، وهو ثنائي ببتيد موجود في العضلات الهيكلية.
في الفطريات Actinomycetota والفطريات الخيطية ، مثل Neurospora crassa ، يمكن تحويل الهيستدين إلى إرغوثيونين المضاد للأكسدة.
متطلبات
حدد مجلس الغذاء والتغذية (FNB) التابع للمعهد الأمريكي للطب المخصصات الغذائية الموصى بها (RDAs) للأحماض الأمينية الأساسية في عام 2002.
بالنسبة للهستيدين ، للبالغين 19 عامًا فما فوق ، 14 مجم / كجم من وزن الجسم / يوم.