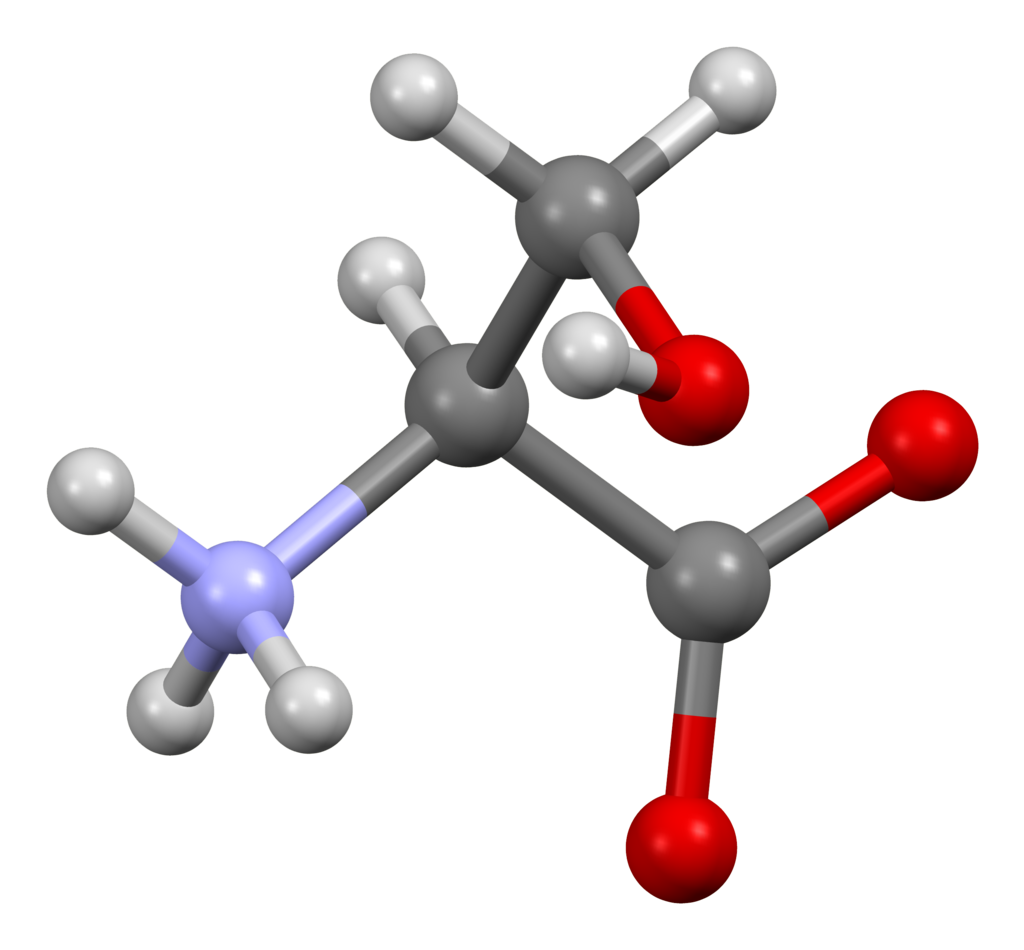
سيرين (رمز Ser أو S) هو حمض أميني ألفا يستخدم في التخليق الحيوي للبروتينات. يحتوي على مجموعة α-amino (الموجودة في البروتونات −NH+
3 في ظل الظروف البيولوجية) ، مجموعة الكربوكسيل (التي هي في −COO− منزوع النواة تشكل تحت الظروف البيولوجية) ، وسلسلة جانبية تتكون من مجموعة هيدروكسي ميثيل ، وتصنفها على أنها حمض أميني قطبي.
يمكن تصنيعه في جسم الإنسان في ظل الظروف الفسيولوجية العادية ، مما يجعله من الأحماض الأمينية غير الأساسية.
يتم ترميزه بواسطة الأكواد UCU و UCC و UCA و UCG و AGU و AGC.
هذا المركب هو أحد الأحماض الأمينية المكونة للبروتين بشكل طبيعي. فقط L-stereoisomer يظهر بشكل طبيعي في البروتينات. إنه ليس ضروريًا للنظام الغذائي للإنسان ، حيث يتم تصنيعه في الجسم من مستقلبات أخرى ، بما في ذلك الجلايسين. تم الحصول على سيرين لأول مرة من بروتين الحرير ، وهو مصدر غني بشكل خاص ، في عام 1865 بواسطة إميل كريمر. اسمها مشتق من اللاتينية للحرير ، sericum. تم إنشاء هيكل سيرين في عام 1902. تشمل المصادر الغذائية التي تحتوي على نسبة عالية من L-Serine بين البروتينات البيض ، والادامامي ، ولحم الضأن ، والكبد ، ولحم الخنزير ، والسلمون ، والسردين ، والأعشاب البحرية ، والتوفو.
التخليق الحيوي
يبدأ التخليق الحيوي للسيرين بأكسدة 3-فوسفوجليسيرات (وسيط من تحلل السكر) إلى 3-فوسفوهيدروكسي بيروفات و NADH بواسطة نازعة هيدروجين الفوسفوجليسيرات (EC 1.1.1.95). ينتج عن التحسين الاختزالي (النقل) لهذا الكيتون بواسطة ترانساميناز الفوسفوسرين (EC 2.6.1.52) 3-فوسفوسرين (O-phosphoserine) الذي يتحلل إلى سيرين بواسطة فسفاتيز الفوسفوسرين (EC 3.1.3.3).
في بكتيريا مثل الإشريكية القولونية ، يتم ترميز هذه الإنزيمات بواسطة الجينات serA (EC 1.1.1.95) ، و serC (EC 2.6.1.52) ، و serB (EC 3.1.3.3).
التخليق الحيوي للجليسين: سيرين هيدروكسي ميثيل ترانسفيراز (SHMT = سيرين ترانسهيدروكسي ميثيلاز) يحفز أيضًا التحويلات القابلة للعكس من L-serine إلى الجلايسين (الانقسام الرجعي للألدول) و 5،6،7،8-tetrahydrofolate إلى 5،10 -THylenetrahydrofolate . [12] SHMT هو إنزيم يعتمد على بيريدوكسال فوسفات (PLP). يمكن أيضًا تكوين الجلايسين من CO2 و NH4 + و mTHF في تفاعل محفز بواسطة سينسيز الجلايسين.
الوظيفة البيولوجية
الأيض
السيرين مهم في عملية التمثيل الغذائي لأنه يشارك في التخليق الحيوي للبيورينات والبيريميدين. إنه مقدمة للعديد من الأحماض الأمينية بما في ذلك الجلايسين والسيستين ، وكذلك التربتوفان في البكتيريا. وهو أيضًا مقدمة للعديد من المستقلبات الأخرى ، بما في ذلك السفينجوليبيدات والفولات ، وهو المتبرع الرئيسي لشظايا الكربون الواحد في التخليق الحيوي.
إرسال الإشارات
يعمل D-Serine ، المُصنَّع في الخلايا العصبية بواسطة إنزيم السيرين Racemase من L-serine (المتماثل الخاص به) ، كمُعدِّل عصبي عن طريق تنشيط مستقبلات NMDA ، مما يجعلها قادرة على الانفتاح إذا ارتبطت أيضًا بالجلوتامات. D-serine هو ناهض قوي في موقع الجلايسين (NR1) لمستقبلات الغلوتامات من النوع NMDA (NMDAR). لكي يفتح المستقبل ، يجب أن يرتبط الجلوتامات وإما الجلايسين أو D- سيرين به ؛ بالإضافة إلى ذلك ، يجب عدم تقييد مانع المسام (مثل Mg2 + أو Zn2 +). في الواقع ، D-serine هو ناهض أقوى في موقع الجلايسين على NMDAR من الجلايسين نفسه.
كان يعتقد أن D-serine موجود فقط في البكتيريا حتى وقت قريب نسبيًا. كان ثاني حمض أميني D اكتشف بشكل طبيعي في البشر ، موجود كجزيء إشارة في الدماغ ، بعد وقت قصير من اكتشاف D-aspartate. إذا تم اكتشاف الأحماض الأمينية D في البشر في وقت مبكر ، فقد يتم بدلاً من ذلك تسمية موقع الجلايسين على مستقبل NMDA بموقع D-serine.
بصرف النظر عن الجهاز العصبي المركزي ، يلعب D-serine دورًا في إرسال الإشارات في الأنسجة والأعضاء الطرفية مثل الغضاريف والكلى والجسم الكهفي.
الأهمية السريرية
اضطرابات عوز السيرين هي عيوب نادرة في التخليق الحيوي للحمض الأميني L- سيرين.
في الوقت الحاضر تم الإبلاغ عن ثلاثة اضطرابات:
- نقص هيدروجيناز 3- فوسفوجليسيرات
- نقص إنزيم 3- فوسفاتيز
- نقص فسفوسرين أمينوترانسفيراز
تؤدي عيوب الإنزيم هذه إلى أعراض عصبية شديدة مثل صغر الرأس الخلقي والتخلف الحركي النفسي الشديد ، بالإضافة إلى حدوث نوبات مستعصية في المرضى الذين يعانون من نقص 3-فوسفوجليسيرات ديهيدروجينيز.
تستجيب هذه الأعراض إلى درجة متفاوتة للعلاج بـ L-serine ، وأحيانًا يتم دمجها مع الجلايسين.
الاستجابة للعلاج متغيرة والنتيجة طويلة الأجل والوظيفية غير معروفة.
لتوفير أساس لتحسين فهم ارتباط الوبائيات والنمط الوراثي / النمط الظاهري ونتائج هذه الأمراض وتأثيرها على نوعية حياة المرضى ، وكذلك لتقييم الاستراتيجيات التشخيصية والعلاجية ، تم إنشاء سجل للمرضى من قبل منظمة العمل الدولية غير التجارية. مجموعة الاضطرابات ذات الصلة بالناقلات العصبية (iNTD).
البحث عن الاستخدام العلاجي
تم اعتبار تصنيف L-serine على أنه حمض أميني غير أساسي شرطيًا ، نظرًا لأن الفقاريات مثل البشر لا يمكنها دائمًا تجميع الكميات المثلى على مدار حياتها بأكملها.
تم إثبات سلامة L-serine في المرحلة الأولى من التجربة السريرية البشرية المعتمدة من قِبل إدارة الأغذية والعقاقير (FDA) مع التصلب الجانبي الضموري (Amyotrophic Lateral Sclerosis)، مرضى ALS (ClinicalTrials.gov معرف: NCT01835782) ، ولكن علاج أعراض ALS لم يتم بعد مبين.
وجد التحليل التلوي لعام 2011 أن الساركوزين المساعد له حجم تأثير متوسط للأعراض السلبية والشاملة.
هناك أيضًا دليل على أن L-serine يمكن أن يكتسب دورًا علاجيًا في مرض السكري.
تتم دراسة دي-سيرين في القوارض كعلاج محتمل لمرض انفصام الشخصية.
تم وصف D-Serine أيضًا على أنه مؤشر حيوي محتمل للتشخيص المبكر لمرض الزهايمر (AD) ، نظرًا لتركيزه المرتفع نسبيًا في السائل النخاعي لمرضى الزهايمر المحتملين.
تم وضع نظرية دي سيرين كعلاج محتمل لاضطرابات السمع الحسي العصبي مثل فقدان السمع وطنين الأذن.